|
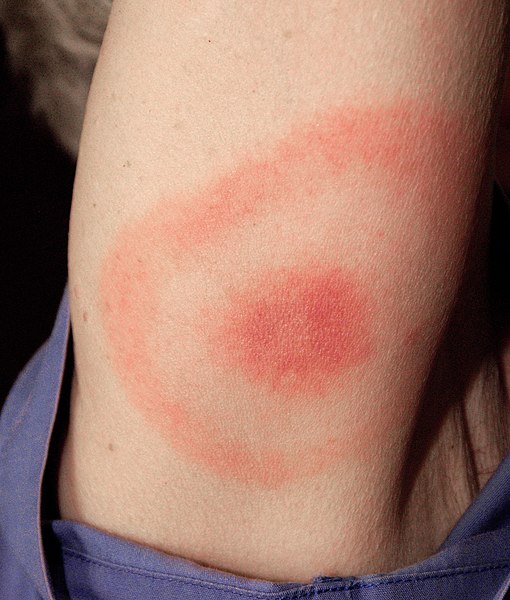
Helicobacter heilmannii
|
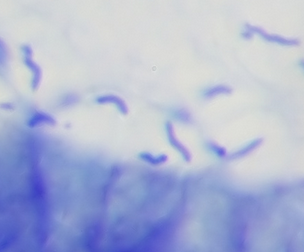
Helicobacter heilmannii ist ein gramnegatives, mikroaerophiles, spiralförmiges Bakterium, das seltener als Helicobacter pylori den Magen des Menschen besiedelt. Es ist vor allem bei Tieren (z. B. Hunde, Katzen, Schweine) verbreitet und wird als zoonotischer Erreger betrachtet.
Pathogenese
- Weniger virulente Faktoren als H. pylori, aber ähnliche Pathogenitätsmechanismen
- Chronische gastrische Inflammation, jedoch geringere Assoziation mit Ulkuskrankheit
- Wird mit gastrointestinalen Lymphomen (MALT-Lymphomen) in Verbindung gebracht
Assoziierte Erkrankungen
Diagnostik
Therapie
- Eradikation wie bei H. pylori mit Triple- oder Quadruple-Therapie
- Therapieindikation insbesondere bei MALT-Lymphomen oder symptomatischer Gastritis
- Zoonotische Infektionsquelle beachten (Tierkontakte reduzieren)
Synonyms -
H. heilmannii,H. heilmannii-Bakterien
|
|
Helicobacter pylori
|
Helicobacter pylori ist ein gramnegatives, mikroaerophiles, spiralförmiges Bakterium, das die Magenschleimhaut besiedelt und eine zentrale Rolle in der Pathogenese von gastrischen Erkrankungen spielt.
Pathogenese
- Produktion von Urease → Spaltung von Harnstoff in Ammoniak → Neutralisation der Magensäure
- Induktion chronischer Gastritis durch zunehmende Schleimhautentzündung
- Veränderung der epithelialen Signalwege durch CagA- und VacA-Toxine
Assoziierte Erkrankungen
Diagnostik
- Invasive Methoden: Histologie, Urease-Schnelltest, Kultur
- Nicht-invasive Methoden: H. pylori-Antigentest im Stuhl, C13-Harnstoff-Atemtest, Serologie
Therapie
Synonyms -
H. pylori
|
|
Helicobacter pylori – Eradikation
|
Die Helicobacter pylori-Eradikation bezeichnet die vollständige Entfernung des Bakteriums H. pylori aus der Magenschleimhaut durch eine gezielte Antibiotikatherapie. Ziel ist die Behandlung oder Prävention von chronischer Gastritis, peptischen Ulzera, MALT-Lymphomen und Magenkarzinomen.
Therapie
Klinische Bedeutung
- Eradikation führt zur Heilung gastrischer Ulzera und Regression von MALT-Lymphomen im Frühstadium
- Reduktion des Risikos für Magenkarzinome, insbesondere bei chronischer Gastritis
Helicobacter heilmannii
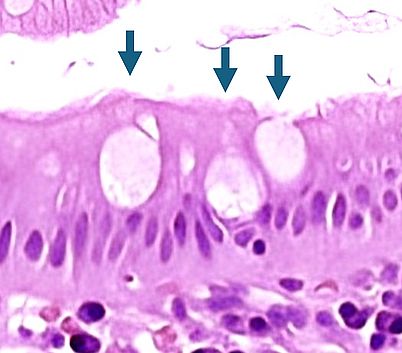
H. heilmannii ist eine seltenere, zoonotische Helicobacter-Spezies (häufig aus Katzen, Hunden), die ebenfalls chronische Gastritis, Ulzera und MALT-Lymphome verursachen kann. Histologisch zeigt sich häufig eine dichte Besiedelung der Magenfoveolen mit langen, gewundenen Bakterien. Die Therapie orientiert sich an der H. pylori-Eradikation, obwohl spezifische Resistenzdaten begrenzt sind.
Synonyms -
Eradikation
|
|
HER2
|
HER2 (Human Epidermal Growth Factor Receptor 2, syn. HER2/neu, Chromosom 17q12) ist eine membranständige Tyrosinkinase aus der HER/ERBB-Familie. Im Gegensatz zu anderen HER-Rezeptoren hat HER2 keine direkten Liganden, sondern wird durch **Heterodimerisierung** mit anderen ERBB-Rezeptoren aktiviert. Es spielt eine zentrale Rolle in Zellproliferation, Überleben und Differenzierung.
Pathologische Relevanz
- HER2-Überexpression/Amplifikation: Führt zu gesteigerter Signaltransduktion und ist ein Treiber in verschiedenen Karzinomen.
- HER2-positives Mammakarzinom: In ca. 15–20 % der Fälle nachweisbar, assoziiert mit aggressiverem Verlauf.
- HER2-positives Magenkarzinom: In ca. 10–20 % der Fälle vorhanden, wichtiger Biomarker für zielgerichtete Therapie.
- HER2-Mutationen in anderen Tumoren: Punktmutationen oder Amplifikationen z. B. bei Kolorektal- und Lungenkarzinomen, potenziell therapierbar.
Diagnostik
- Nachweis der HER2-Expression mittels Immunhistochemie (IHC), Bewertung nach 0–3+ Score.
- FISH (Fluoreszenz-in-situ-Hybridisierung) oder CISH (Chromogenic in-situ Hybridization) zur Bestätigung einer Amplifikation bei IHC 2+.
- NGS zur Detektion von HER2-Mutationen in seltenen Tumoren.
Therapeutische Relevanz
- Monoklonale Antikörper: Trastuzumab, Pertuzumab (HER2-positives Mammakarzinom, Magenkarzinom).
- Antikörper-Wirkstoff-Konjugate: Trastuzumab-Emtansin (T-DM1), Trastuzumab-Deruxtecan (T-DXd).
- Tyrosinkinase-Inhibitoren: Lapatinib, Neratinib (HER2-aktivierte Karzinome).
- HER2-Mutationen: Potenzielles Ziel für Neratinib und andere Inhibitoren bei HER2-mutierten Tumoren.
Synonyms -
HER2/neu
|
|
Herz
|
Das Herz (Gewicht ca. 250-350g) ist ein muskuläres Hohlorgan im Mediastinum, das als zentrale Druck- und Saugpumpe den systemischen und pulmonalen Blutkreislauf aufrechterhält. Es besteht aus vier Kammern (rechter/linker Vorhof und Ventrikel) und ist rhythmisch-autonom aktiv (Sinusknoten).
Wandschichten
- Endokard: Innenschicht aus Endothel, bildet auch die Herzklappen
- Myokard: Herzmuskelschicht (links 10-15mm, rechts 3-5mm Dicke)
- Epikard: Äußere Schicht, mit Perikard verwachsen
Herzmuskulatur (Histologie)
- Quergestreift, einkernig, verzweigt, Glanzstreifen (Disci intercalares)
Koronargefäße
- A. coronaria dextra & sinistra: Versorgen Myokard mit O2
- Abgänge: RIVA, RCX, R. interventricularis posterior
- Venös: Sinus coronarius mündet in rechten Vorhof
Erregungsleitung
- Sinusknoten → AV-Knoten → His-Bündel → Tawara-Schenkel → Purkinje-Fasern
Pathologische Relevanz
- Myokardinfarkt: Ischämische Koagulationsnekrose
- Myokarditis: Lymphozytär (viral), eosinophil, Riesenzellig
- Kardiomyopathien: Dilatativ, hypertroph, restriktiv – teils genetisch
- Klappenerkrankungen: Degenerativ, rheumatisch, infektiös (Endokarditis)
Diagnostik
- Histopathologie: Endomyokardbiopsie (z. B. bei Myokarditis oder Transplantatabstoßung)
- Serummarker: Troponin T/I, CK-MB bei Myokardschädigung
- Bildgebung: Echo, CT, MRT – strukturelle und funktionelle Analyse
Synonyms -
kardial
|
|
HGF/MET-Signalweg
|
Der MET-Signalweg wird durch den Hepatozyten-Wachstumsfaktor (HGF) aktiviert und reguliert Zellproliferation, Migration, Differenzierung und Überleben. Der zugehörige Rezeptor c-Met wird durch das MET-Gen (7q31.2) kodiert und gehört zur Familie der Rezeptor-Tyrosinkinasen (RTKs).
Aktivierung des Signalwegs
- HGF bindet an c-Met → Rezeptordimerisierung → Autophosphorylierung
- Rekrutierung von Signalproteinen wie GRB2, GAB1 und PI3K
- Aktivierung nachgeschalteter Signalwege:
- RAS/MAPK → Zellproliferation
- PI3K/AKT → Zellüberleben, Anti-Apoptose
- STAT3 → Zellmigration und Invasion
Pathologische Relevanz
- MET-Amplifikationen oder MET-Exon-14-Skipping-Mutationen führen zur konstitutiven Aktivierung des Signalwegs.
- Häufig bei nicht-kleinzelligem Lungenkarzinom (NSCLC), Gastrointestinalen Tumoren und Glioblastomen.
Therapeutische Relevanz
- Tyrosinkinase-Inhibitoren (TKIs): Capmatinib, Tepotinib und Crizotinib hemmen den MET-Signalweg.
- Gezielte Therapien verbessern die Prognose bei MET-alterierten Tumoren.
Synonyms -
MET-Signalwegs
|
|
Histologie
|
Histologie (griech. histos = Gewebe, logos = Lehre) ist die Lehre vom mikroskopischen Aufbau biologischer Gewebe. Sie stellt ein zentrales Teilgebiet der Pathologie und Anatomie dar und dient der Untersuchung von Zell- und Gewebestrukturen mittels Licht- und Elektronenmikroskopie.
Teilgebiete
- Allgemeine Histologie: Untersuchung grundlegender Gewebearten (z. B. Epithel-, Muskel-, Binde- und Nervengewebe)
- Spezielle Histologie: Organbezogene Gewebestrukturen (z. B. Leberläppchen, Glomeruli, Bronchialepithel)
Methoden
- Fixierung: Z. B. Formalin zur Konservierung
- Einbettung: Meist Paraffin, alternativ Kunststoff
- Schnitttechnik: Mikrotom-Schnitte mit 2–5 µm Dicke
- Färbungen:
- Standard: Hämatoxylin-Eosin (H.E.)
- Spezialfärbungen: PAS, Trichrom, Silberfärbungen
- Immunhistochemie: Nachweis von Proteinen mittels Antikörpern (z. B. Ki-67, p53)
- Elektronenmikroskopie: Für ultrastrukturelle Details (z. B. Basalmembran, Mitochondrien)
Klinische Relevanz
- Zentrale diagnostische Methode in der Pathologie, insbesondere zur Tumorklassifikation
- Beurteilung entzündlicher, degenerativer und neoplastischer Prozesse
- Unverzichtbar in der Transplantations- und Autoimmundiagnostik (z. B. Biopsieauswertung)
- Grundlage für molekulare und immunhistochemische Zusatzanalysen
Synonyms -
Histologische
|
|
Histoplasmose
|
Die Histoplasmose ist eine systemische Mykose, verursacht durch das dimorphe Pilzpathogen Histoplasma capsulatum. Die Infektion erfolgt meist inhalativ über kontaminierten Staub (z. B. Vogelkot, Fledermauskot) und betrifft vor allem Lunge und retikuloendotheliales System.
Erreger
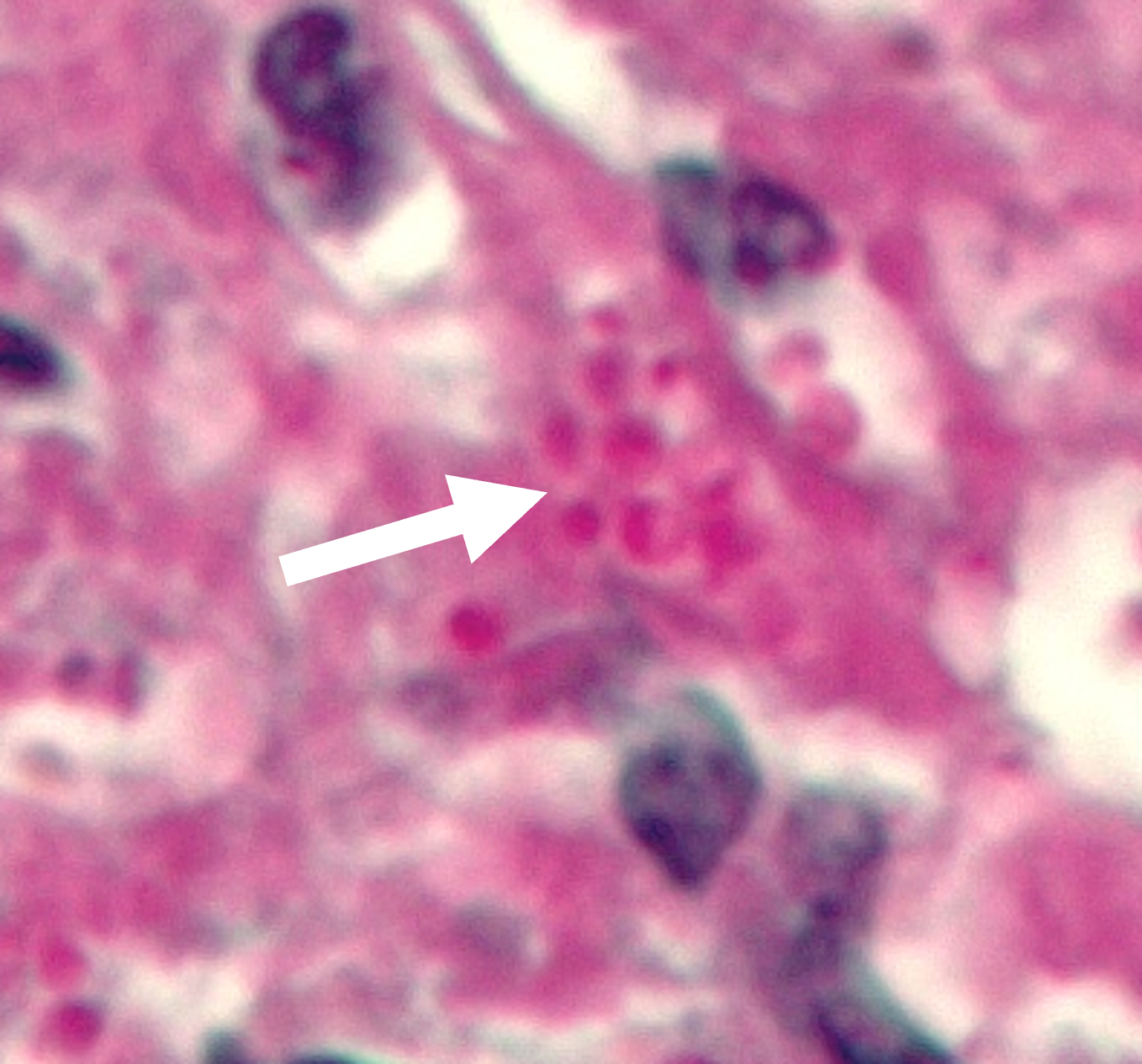
- Histoplasma capsulatum: Dimorpher Pilz – in Gewebe als intrazelluläre Hefezellen, in Kultur als Schimmelpilz
- Vorkommen v. a. in Nord-, Mittel- und Südamerika, Afrika und Asien
Histologie
Klinische Manifestation
Diagnostik und Relevanz
- Histologie: Intrazelluläre Hefen im Kontext nekrotisierender Entzündung
- Kultur, Antigennachweis im Urin oder Serum
- Therapie: Itraconazol, bei schwerer Verlaufsform Amphotericin B
|
|
Hormon
|
Hormone sind biochemische Botenstoffe, die von spezialisierten Zellen (meist endokrinen Drüsen) produziert und über den Blutkreislauf zu Zielzellen transportiert werden. Dort regulieren sie zahlreiche physiologische Prozesse wie Stoffwechsel, Wachstum, Reproduktion und Homöostase.
Klassifikation
- Peptidhormone: z. B. Insulin, Parathormon, ACTH
- Steroidhormone: z. B. Cortisol, Testosteron, Östradiol
- Aminosäurederivate: z. B. Adrenalin, Thyroxin (T4)
Wirkmechanismus
- Bindung an spezifische Rezeptoren auf oder in Zielzellen
- Aktivierung intrazellulärer Signalwege (z. B. cAMP, Tyrosinkinase, Steroidrezeptoren)
- Modulation von Genexpression, Enzymaktivität oder Membrantransportprozessen
Klinische Relevanz
- Hormonstörungen (z. B. Hyperthyreose, Diabetes mellitus, Hypogonadismus) können zahlreiche Organsysteme betreffen
- Viele Tumoren zeigen hormonelle Abhängigkeit (z. B. Mamma-, Prostata-, Schilddrüsenkarzinome)
- Therapeutisch kommen Hormonanaloga, Antagonisten oder Blocker zum Einsatz
Synonyms -
Hormone,hormonabhängig,hormonabhängige,hormonaghängiges,hormonunabhängig,hormununabhängiges,hormonunabhängige, Hormonelle
|
|
Hotspot
|
Ein Hotspot bezeichnet in der Pathologie ein Areal im Gewebepräparat mit maximaler Merkmalsausprägung oder höchster Positivitätsrate bei immunhistochemischen Markern wie Ki-67, p53, PHH3 oder mitotischer Aktivität.
Merkmale
- Hotspots sind fokal begrenzte Zonen mit hoher Teilungsaktivität (Ki-67)
- Sie werden gezielt zur repräsentativen quantitativen Auswertung herangezogen
- Typischerweise unter 200–400× Vergrößerung identifiziert
Beispiel: Ki-67
- Ermittlung des Ki-67-Index durch Zählung von positiven Zellkernen im Hotspot (meist auf 500–1000 Zellen)
- Proliferationsrate kann je nach Tumorentität prognostisch und therapeutisch relevant sein (z. B. Mamma-Ca, NET, Lymphome)
Hinweis
- Die Auswahl des Hotspots erfordert Erfahrung und standardisierte Kriterien
- Bei manchen Tumoren wird zusätzlich eine mittlere Positivitätsrate über das gesamte Areal verlangt
|
|
HOXB13
|
HOXB13 ist ein Gen auf Chromosom 17q21.32, das für einen Homeobox-Transkriptionsfaktor kodiert. Es reguliert die Entwicklung und Differenzierung der Prostata durch Interaktion mit dem Androgenrezeptor.
Bedeutung bei Prostatakrebs
- Die Keimbahnmutation G84E erhöht das Risiko für familiären Prostatakrebs um das 10- bis 20-fache.
- Tritt häufig in nordeuropäischen Populationen auf und ist bei 5 % der familiären Prostatakarzinome nachweisbar.
Klinische Relevanz
- Früherkennung: Genetische Tests auf HOXB13 sind bei familiärem Prostatakrebs entscheidend.
|
|
HPF
|
HPF steht für High Power Field (deutsch: Hochvergrößerungsfeld) und bezeichnet das Sichtfeld eines Mikroskops bei hoher Vergrößerung, typischerweise bei 400-facher Vergrößerung (40x Objektiv, 10x Okular).
Verwendung in der Pathologie
- Dient zur standardisierten Quantifizierung von Zellen oder Strukturen pro Gesichtsfeld
- Wird z. B. zur Bestimmung von Mitosezahlen, eosinophilen Granulozyten, Plasmazellen oder Apoptosen pro HPF genutzt
- Wichtig für die graduelle Einteilung (Grading) und diagnostische Schwellenwerte in der Histopathologie
Technische Hinweise
- Die Fläche eines HPF kann je nach Mikroskop leicht variieren (~0,15–0,25 mm²)
- Zur Vergleichbarkeit ist die Kalibrierung und Dokumentation der HPF-Fläche wichtig (z. B. bei Studien oder Guidelines)
|
|
HSV
|
HSV (Herpes-simplex- Virus) gehört zur Familie der Herpesviridae und umfasst zwei Typen: HSV-1 (oral bevorzugt) und HSV-2 (genital bevorzugt). Beide Virustypen sind DNA-Viren mit neurotropem Verhalten und persistieren nach Erstinfektion lebenslang im Körper.
Pathogenese
- Primärinfektion über Schleimhäute oder Haut
- Retrograder Transport in das periphere Nervensystem und Etablierung einer latenten Infektion in Spinal- oder Hirnnervenganglien
- Reaktivierung durch Stress, Immunsuppression, UV-Licht → rezidivierende Läsionen
Klinische Manifestationen
- HSV-1: Lippenherpes (Herpes labialis), Herpes gingivostomatitis, selten Enzephalitis
- HSV-2: Genitalherpes, perinatale Infektion beim Neugeborenen (Herpes neonatorum)
- Andere: Keratokonjunktivitis, Eczema herpeticatum (bei atopischer Dermatitis), Herpes simplex-Enzephalitis
Histologie
- Ballonierung der Epithelzellen
- Multinukleäre Riesenzellen mit chromatinrandständigen Kernen ("Cowdry-A-Einschlüsse")
- Ulzerationen mit intraepithelialen Bläschen
Diagnostik
- Zytologie (Tzanck-Test), Histologie, PCR, Virusnachweis im Abstrich oder Liquor
Therapie
- Antivirale Medikamente wie Aciclovir, Valaciclovir, Famciclovir
Synonyms -
Herpes simplex Virus
|
|
Hydrophob
|
Hydrophob bedeutet „wasserabweisend“ oder „wassermeidend“ und beschreibt Moleküle oder Molekülbereiche, die sich nicht mit Wasser vermischen bzw. nicht in Wasser löslich sind. Hydrophobe Substanzen besitzen in der Regel keine polaren Gruppen und bilden keine Wasserstoffbrücken mit Wassermolekülen.
Beispiele
- Langkettige Kohlenwasserstoffe (z. B. Fettsäuren, Lipide)
- Membranlipide: Ihre hydrophoben Fettsäurereste lagern sich in Zellmembranen nach innen
Biologische Bedeutung
- Hydrophobe Wechselwirkungen spielen eine wichtige Rolle bei der Proteinstruktur und Membranbildung
- Grundlage für die Ausbildung von Lipid-Doppelschichten biologischer Membranen
Synonyms -
hydophobe,hydrophobes,hydrophober,Hydrophobe
|
|
Hyperämie
|
Hyperämie bezeichnet eine vermehrte Durchblutung eines Gewebes infolge dilatierter Blutgefäße. Sie kann aktiv oder passiv sein und tritt physiologisch (z. B. bei Muskelarbeit) oder pathologisch (z. B. bei Entzündungen) auf.
Formen
- Aktive Hyperämie: Durch Vasodilatation gesteigerter arterieller Zufluss, z. B. bei Entzündung, Wärme, metabolischer Aktivität.
- Passive Hyperämie (Stauung): Durch Abflussbehinderung (z. B. venöser Rückstau) bedingte Blutansammlung im Gewebe.
Histologie
- Erweiterte und mit Erythrozyten prall gefüllte Kapillaren und Venolen
- Oft begleitend: Ödem, initial keine Zellinfiltrate bei reiner Hyperämie
- Bei passiver Hyperämie zusätzlich: Hämosiderinablagerungen, Atrophie, Fibrose (chronisch)
Hyperämie und Entzündung
- Aktive Hyperämie ist ein zentrales Merkmal der akuten Entzündung
- Verursacht das klassische Entzündungszeichen "Rubor" (Rötung) nach Galen
- Zusammen mit "Calor", "Tumor", "Dolor" und "Functio laesa" beschreibt sie die lokalen Entzündungszeichen
Klinische Relevanz
- Hyperämie ist reversibel und Ausdruck gesteigerter Stoffwechselaktivität oder Reaktion auf Gewebsschädigung
- Differenzierung zur passiven Hyperämie (Stauung) ist histologisch und klinisch wichtig
Synonyms -
hyperäm,hyperämisch,Rötung,Rubor,Kapillardilatation
|
/Helicobacter%20pylori-Gastritis/Mikroskopie/H_pylori_REM.jpg)