|
Gain-of-Function-Mutationen
|
Gain-of-Function-Mutationen (GOF) sind genetische Veränderungen, die zu einer verstärkten, konstitutiven oder neuen Funktion eines Proteins führen. Diese Mutationen können die Zellproliferation, Signaltransduktion oder Resistenzmechanismen in Tumorzellen fördern.
Mechanismen
- Erhöhte Aktivität: Verstärkte Enzymfunktion oder Rezeptoraktivierung (z. B. konstitutive Kinaseaktivierung).
- Stabilisierung des Proteins: Verhindert Abbau oder erhöht die Halbwertszeit (z. B. MET-Exon-14-Skipping).
- Neue Funktionen: Änderung der Substratspezifität oder Interaktionen mit neuen Proteinen.
Beispiele in der Onkologie
- EGFR (L858R, Exon-19-Deletionen): Führt zu einer konstitutiven Kinaseaktivität im nicht-kleinzelligen Lungenkarzinom.
- KRAS (G12D, G12C): Dauerhafte Aktivierung des MAPK-Signalwegs in Kolorektal- und Pankreaskarzinomen.
- BRAF (V600E): Hyperaktivierung des MAPK-Signalwegs in Melanomen.
- PIK3CA (H1047R): Verstärkte PI3K-Signalgebung in Brust- und Endometriumkarzinomen.
Klinische Relevanz
- Wichtige Zielstrukturen für Tyrosinkinase-Inhibitoren (TKIs) oder monoklonale Antikörper.
- Prädiktive Marker für die Therapieentscheidung, z. B. KRAS-G12C-Inhibitoren (Sotorasib, Adagrasib).
- Erkennung mittels Next-Generation-Sequencing (NGS) für personalisierte Behandlungsstrategien.
Synonyms -
GoF-Mutationen,GoF-Mutation
|
|
Gallensäure
|
Gallensäuren sind amphiphile Steroide, die in der Leber aus Cholesterin gebildet werden und eine zentrale Rolle bei der Fettverdauung und -resorption im Dünndarm spielen. In konjugierter Form mit Glycin oder Taurin liegen sie im Darm meist als Gallensalze vor.
Primäre und sekundäre Gallensäuren
- Primäre Gallensäuren: Cholsäure, Chenodesoxycholsäure – in der Leber gebildet
- Sekundäre Gallensäuren: Desoxycholsäure, Lithocholsäure – durch bakterielle Umwandlung im Kolon
Funktion
- Emulgieren von Fetten zur Bildung von Mizellen für die Absorption im Dünndarm
- Fördern die Aufnahme von Fettsäuren, Cholesterin und fettlöslichen Vitaminen
- Regulieren den enterohepatischen Kreislauf über FXR und TGR5-Rezeptoren
Klinische Relevanz
- Gallensäureverlust (z. B. bei Ileumresektion) kann zu Gallensäure-Diarrhö führen
- Erhöhte Konzentrationen von sekundären Gallensäuren gelten als tumorbegünstigend im Kolon
- Therapeutisch wird z. B. Ursodesoxycholsäure bei cholestatischen Lebererkrankungen eingesetzt
Synonyms -
Gallensäuren,Gallensalze,Gallensalz
|
|
Gallereflux
|
Gallereflux bezeichnet den Rückfluss von Galle aus dem Duodenum in den Magen (duodenogastraler Reflux) oder bis in die Speiseröhre (biliogaströser bzw. biliös-ösophagealer Reflux). Er tritt meist unabhängig von einer Refluxkrankheit mit Magensäure auf, kann diese jedoch verstärken.
Pathophysiologie
- Verlust der pylorischen Barrierefunktion nach Operationen (z. B. Magenresektion, Billroth-I/II, Ösophagusresektion)
- Störung der Magenmotilität oder erhöhter intraduodenaler Druck
- Galle enthält Gallensäuren und Lysolecithin, die schleimhauttoxisch wirken, besonders in Kombination mit Pepsin und Magensäure
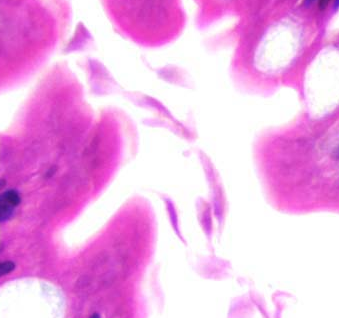
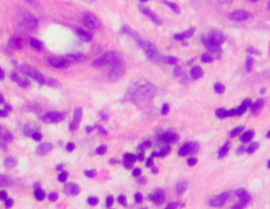
Histologie
Klinische Relevanz
- Symptome: Epigastrische Schmerzen, Übelkeit, Gallenerbrechen, Völlegefühl
- Kann zur biliären Refluxgastritis und im Langzeitverlauf zu Schleimhautveränderungen mit erhöhtem Karzinomrisiko führen
- Diagnose durch Gastroskopie, pH-Metrie und Bilirubin-Messung (z. B. Bilitec)
- Therapie: Prokinetika, Gallensäurebinder, in schweren Fällen operative Rekonstruktion
|
|
Gastrektomie
|
Gastrektomie bezeichnet die operative Entfernung des Magens. Je nach Ausmaß unterscheidet man zwischen partieller (Teilentfernung) und totaler Gastrektomie (vollständige Magenresektion). Die Operation wird bei malignen Tumoren, Therapie-refraktären Ulzera oder massiven Blutungen durchgeführt.
Indikationen
- Magenkarzinom (z. B. Adenokarzinom, Siegelringzellkarzinom)
- Gastrointestinale Stromatumoren (GIST)
- Ulkuskomplikationen: Perforation, Blutung, Penetration
- Bariatrische Chirurgie: selten, z. B. bei metabolischem Versagen nach Sleeve-Gastrektomie
Operationsformen
- Totale Gastrektomie: Entfernung des gesamten Magens inkl. Kardia und Pylorus
- Distale Gastrektomie: Resektion des unteren Magenanteils (z. B. bei Antrumkarzinomen)
- Proximale Gastrektomie: Entfernung des oberen Magenanteils (seltener)
Rekonstruktionsverfahren
- Roux-en-Y-Ösophagojejunostomie: Häufig nach totaler Gastrektomie
- Billroth-I/II: Nach partieller Resektion
Pathologische Relevanz bei Tumoren
- Untersuchung von Resektat, Resektionsrändern und Lymphknoten entscheidend für das Tumorstadium
- Beurteilung von Infiltrationstiefe (pT), Lymphangiosis, Perineuralscheideninvasion
- Histologischer Subtyp nach WHO- oder Laurén-Klassifikation bei Magenkarzinomen
Komplikationen und Spätfolgen
- Dumping-Syndrom (früh oder spät)
- Mangelernährung: insbesondere Vitamin B12-, Eisen- und Kalziummangel
- Refluxösophagitis oder Anastomosenstenosen
|
|
Gastrin
|
Gastrin ist ein gastrointestinales Peptidhormon, das hauptsächlich von den G-Zellen im Antrum des Magens produziert wird. Es stimuliert die Magensaftsekretion, fördert die mukosale Proliferation und erhöht die Magenmotilität.
Pathologische Relevanz
- Erhöht bei chronischer Gastritis Typ A (Autoimmungastritis, Korpusbetont): Hypochlorhydrie → Feedback-induzierte Gastrinerhöhung.
- Niedriger bei chronischer Gastritis Typ B (H. pylori, Antrumbetont): Normo- oder Hyperchlorhydrie mit reduzierter Gastrinfreisetzung.
- Gastrinom / Zollinger-Ellison-Syndrom: Pathologisch erhöhte Gastrinsekretion durch neuroendokrinen Tumor (meist Duodenum oder Pankreas) → Übersäuerung, Ulzera.
Nutzung in der Pathologie
- Immunhistochemischer Nachweis von Gastrin in G-Zellen zur Abgrenzung von Antrum- vs. Korpusmukosa in Biopsien (Gastrin+ = Antrumtypisch).
- Erhöhte Gastrinspiegel im Serum als diagnostischer Hinweis bei Autoimmungastritis oder Gastrinom.
- Unterscheidung der Gastritis-Typen sowie Lokalisation und Typisierung von neuroendokrinen Tumoren.
Synonyms -
Gastrin-Überstimulation,Gastrinerhöhung,Hypergastrinämie
|
|
Gastritis
|
Gastritis bezeichnet eine entzündliche Veränderung der Magenschleimhaut, die akut oder chronisch verlaufen kann. Sie kann durch Infektionen, Autoimmunprozesse, Medikamente oder toxische Substanzen ausgelöst werden und zeigt unterschiedliche histopathologische Muster je nach Ursache.
Ätiologie und Einteilung
Histopathologie
Klinische Relevanz
|
|
Gefäßpathologie
|
Gefäßpathologie befasst sich mit strukturellen und funktionellen Veränderungen der Blut- und Lymphgefäße, die zu hämodynamischen Störungen und Gewebeschädigungen führen können.
Hauptformen der Gefäßpathologien
- Arteriosklerose: Chronisch-progrediente Ablagerung von Lipiden, Entzündungszellen und Bindegewebe in der Intima → Gefäßverengung, Thromboserisiko.
- Vaskulitis: Entzündliche Gefäßerkrankungen durch Autoimmunreaktionen oder Infektionen (z. B. Riesenzellarteriitis, ANCA-assoziierte Vaskulitiden).
- Aneurysmen: Pathologische Erweiterung der Gefäßwand mit Risiko für Ruptur (z. B. Bauchaortenaneurysma).
- Thrombose und Embolie: Gefäßverschluss durch intravasale Gerinnselbildung, häufig in tiefen Beinvenen oder als arterielle Emboliequelle.
- Hypertonie-bedingte Gefäßveränderungen: Hyaline Arteriolosklerose, Mediaverdickung und endotheliale Dysfunktion.
Histopathologische Merkmale
- Arteriosklerotische Plaques mit Lipidkern, Schaumzellen und fibröser Kappe.
- Leukozyteninfiltrate bei Vaskulitiden, oft mit Gefäßnekrose.
- Thromben mit Plättchenaggregaten und fibrinreicher Struktur.
Klinische Relevanz
- Gefäßpathologien sind Hauptursache für Herzinfarkt, Schlaganfall und periphere arterielle Verschlusskrankheit (pAVK).
- Therapieansätze umfassen Lipid- und Blutdrucksenker, Gerinnungshemmung sowie interventionelle Verfahren (z. B. Stents, Bypass-Operation).
|
|
Genetische Prädisposition
|
Genetische Prädisposition bezeichnet die erbliche Veranlagung für die Entwicklung bestimmter Erkrankungen aufgrund genetischer Veränderungen. In der Pathologie spielt sie eine zentrale Rolle bei der Entstehung von Tumoren und anderen erblich bedingten Krankheitsbildern.
Mechanismen
- Vererbung von Keimbahnmutationen in Tumorsuppressorgenen (z. B. BRCA1/2 bei Brust- und Eierstockkrebs)
- Defekte in DNA-Reparaturmechanismen (z. B. MLH1, MSH2 beim Lynch-Syndrom)
- Genetische Syndrome mit erhöhtem Tumorrisiko (z. B. Li-Fraumeni-Syndrom, FAP)
Beispiele für erblich bedingte Tumorprädispositionen
Klinische Relevanz
- Identifikation genetischer Prädispositionen zur Risikostratifizierung
- Gezielte Früherkennungsmaßnahmen und surveillancemethoden (z. B. regelmäßige Koloskopien bei FAP)
- Personalisierte Therapieansätze, z. B. Einsatz von PARP-Inhibitoren bei BRCA-mutierten Tumoren
Synonyms -
genetische Prädisposition
|
|
genomische Instabilität
|
Genomische Instabilität bezeichnet die erhöhte Anfälligkeit von Zellen für genetische Veränderungen wie Mutationen, Chromosomenaberrationen oder epigenetische Modifikationen. Sie entsteht durch Defekte in DNA-Reparaturmechanismen, Zellzykluskontrolle oder Apoptose und ist ein zentrales Merkmal der Tumorentstehung. In der Pathologie fördert sie die intratumorale Heterogenität, Tumorprogression und Therapieresistenz. Diagnostisch wird sie z. B. durch Mikrosatelliteninstabilität (MSI) oder chromosomale Instabilität (CIN) erfasst und beeinflusst die Wahl personalisierter Therapien.
|
|
Gewichtsverlust
|
Gewichtsverlust bezeichnet eine gewollte oder ungewollte Abnahme des Körpergewichts um mehr als 5 % innerhalb von 6–12 Monaten. Er ist ein unspezifisches, aber häufig klinisch bedeutsames Symptom.
Hauptursachen
- Tumorerkrankungen: z. B. Tumorkachexie
- Chronisch-entzündliche Erkrankungen: z. B. Tuberkulose, HIV
- Endokrinologisch: z. B. Hyperthyreose, Diabetes mellitus Typ 1
- Psychisch: Depression, Anorexia nervosa
- Malassimilation: z. B. Zöliakie, Morbus Crohn
Pathophysiologie
- Erhöhter Energieverbrauch und Katabolismus
- Appetitlosigkeit durch Zytokinwirkung (z. B. TNF-α)
- Malabsorption trotz ausreichender Zufuhr
Klinische Relevanz
- Frühsymptom bei Malignomen oder chronischen Erkrankungen
- Wichtiges Warnzeichen bei älteren oder multimorbiden Patienten
- Erfordert gezielte Abklärung der Ursache
|
|
Giardiasis
|
Die Giardiasis ist eine protozoäre Dünndarminfektion, verursacht durch Giardia lamblia (auch: G. intestinalis, G. duodenalis). Sie ist eine der häufigsten parasitären Durchfallerkrankungen weltweit und tritt besonders bei Kindern, Reisenden und immungeschwächten Personen auf.
Erreger, Übertragung und Vorkommen
- Erreger: Giardia lamblia – Flagellat mit Trophozoiten- und Zystenform
- Übertragung: Fäkal-oral durch kontaminiertes Wasser, Lebensmittel oder direkten Kontakt
- Vorkommen: Weltweit, besonders in Entwicklungsländern sowie in Kinderkrippen, Lagern, nach Auslandsreisen („Reisediarrhö“)
- Reservoir: Mensch ist Hauptwirt; selten zoonotische Übertragung von Haustieren (v. a. Hunde, Katzen bei Assemblage A/B)
Histologie
- Trophozoiten: Birnenförmig, 2 Zellkerne („Eulenaugen“), haften an Mukosaepithel
- Kein Gewebeinvasion, aber Mikrovillusatrophie und Malabsorption
- Nachweis mit Giemsa, PAS, Immunfärbungen; histologisch oft nur unspezifisch
Klinische Manifestationen
Diagnostik und Relevanz
|
|
Giemsa-Färbung
|
Die Giemsa-Färbung ist eine polychrome histologische und zytologische Färbung, die zur Darstellung von Zellkernen, Zytoplasma und Mikroorganismen wie Helicobacter pylori, Parasiten und Blutzellen verwendet wird. Sie eignet sich für Gewebeschnitte und Ausstriche.
Färbeprinzip
- Kombination aus Azurfarbstoffen, Methylenblau und Eosin
- Basische Strukturen (z. B. DNA) binden saure Farbstoffe → blau-violett
- Säurehaltige Strukturen (z. B. Zytoplasma) binden basische Farbstoffe → rosa bis hellblau
Typische Färbemuster
Diagnostische Relevanz
Klinische Anwendungen
- Magen: Nachweis von Helicobacter pylori (zusätzlich zu IHC/PAS)
- Hämatologie: Differentialblutbild, Blastenanalyse
- Infektiologie: Nachweis von Plasmodien, Leishmanien, Trypanosomen
Synonyms -
Giemsa
|
|
Grading
|
Grading bezeichnet in der Pathologie die histologische Einstufung der Bösartigkeit eines Tumors anhand seines Differenzierungsgrades und anderer mikroskopischer Merkmale. Beim Grading werden Tumoren in verschiedene Grade eingeteilt (häufig Grad 1 bis 3 oder 4), wobei niedrige Grade (z. B. Grad 1) auf gut differenzierte, weniger aggressive Tumoren und hohe Grade (z. B. Grad 3 oder 4) auf schlecht differenzierte, aggressivere Tumoren hinweisen. Das Grading dient dazu, das Wachstumspotential und die Prognose des Tumors zu beurteilen und kann die Therapieplanung beeinflussen.
|
|
Granulationsgewebe
|
Granulationsgewebe ist ein provisorisches, hochvaskularisiertes Bindegewebe, das im Rahmen der Wundheilung gebildet wird. Es entsteht in der proliferativen Phase der Heilung und dient als Übergangsstruktur zur Narbenbildung.
Histologische Merkmale
- Fibroblasten: Synthese von Kollagen und extrazellulärer Matrix.
- Kapilläre Neubildung (Angiogenese): Dichtes Netzwerk aus neu gebildeten, oft undichten Kapillaren.
- Entzündungszellen: Makrophagen, Lymphozyten und Plasmazellen zur Wundreinigung und Regulation.
- Ödem: Aufgrund der erhöhten Gefäßpermeabilität.
Funktion
- Bereitet das Gewebe auf die Geweberegeneration oder Narbenbildung vor.
- Fördert die Gefäßneubildung für Nährstoff- und Sauerstoffversorgung.
- Unterstützt die Einwanderung von Epithelzellen zur Wunddeckung.
- Wächst in Nekrosen oder Infarktareale ein und baut diese ab.
Klinische Relevanz
- Physiologische Wundheilung: Abbau und Umwandlung in reifes Bindegewebe.
- Chronische Wunden: Persistierendes Granulationsgewebe bei gestörter Heilung.
- Pathologische Narbenbildung: Überschießende Granulation kann zur Keloidbildung führen.
|
|
Granulom
|
Granulome sind umschriebene Ansammlungen aktivierter Makrophagen (Epitheloidzellen), die im Rahmen einer chronisch-entzündlichen Immunreaktion auftreten. Sie dienen der Abkapselung persistierender Reize wie Erreger, Fremdkörper oder Autoantigene.
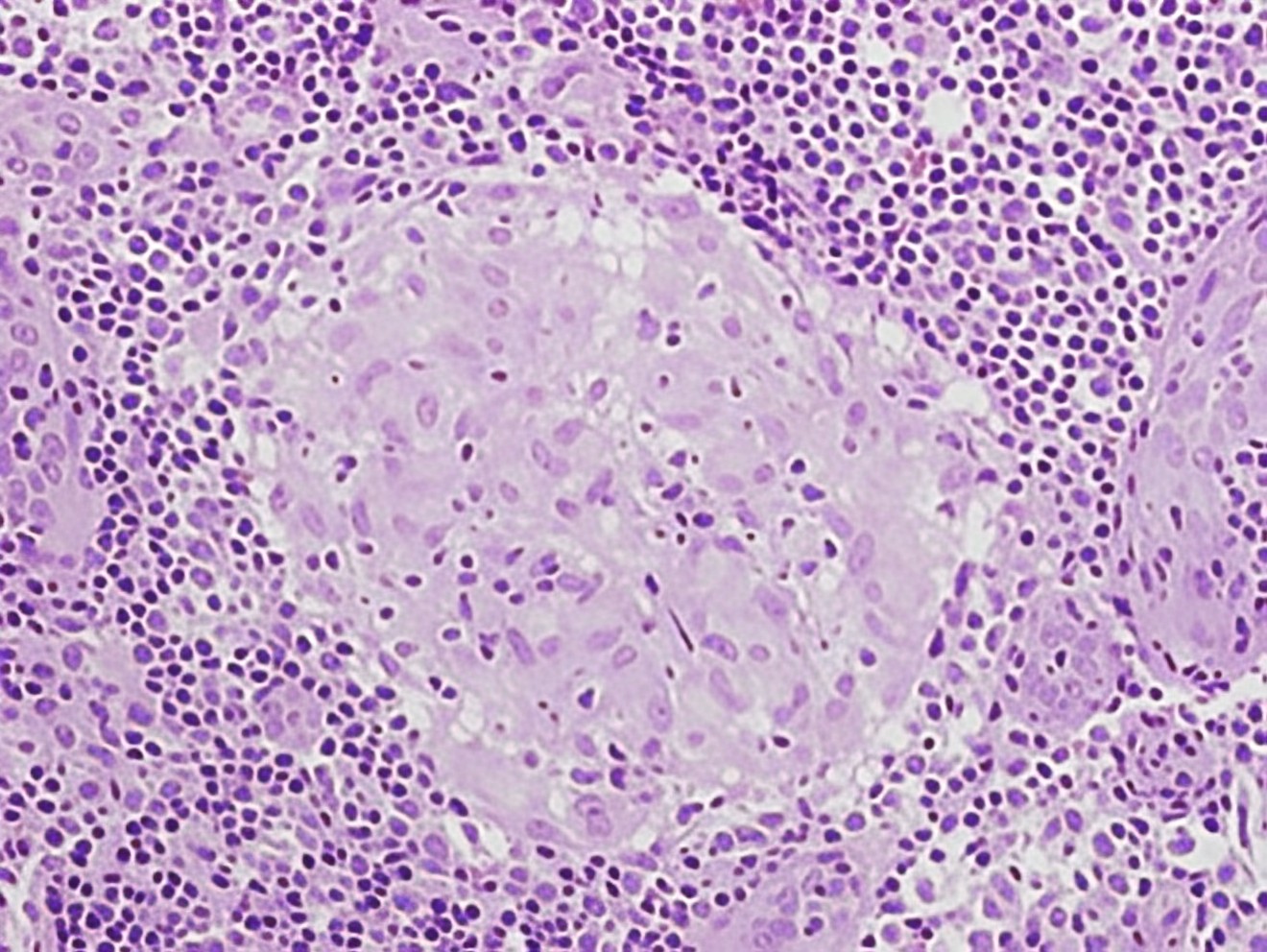
Histologie
- Zentrale Epitheloidzellen ± mehrkernige Riesenzellen, umgeben von Lymphozyten.
- Verkäsend (mit zentraler Nekrose) oder nicht-verkäsend, je nach Ursache.
Pathogenese und Zytokinvermittelung
- Auslösung durch persistente Antigene, die eine chronische Aktivierung des Immunsystems bewirken.
- Wichtige Zytokine: IFN-γ (von Th1-Zellen) → aktiviert Makrophagen; TNF-α → unterstützt Granulombildung und Erhaltung; IL-12 → fördert Th1-Antwort.
- Granulombildung ist ein zellulär-immunvermittelter Prozess, dominiert von Makrophagen und T-Helferzellen.
Ursachen (mit Granulomtyp)
- Tuberkulose: verkäsend (Mykobakterien).
- Sarkoidose, Crohn: nicht-verkäsend.
- Fremdkörper: nicht-verkäsend, oft mit Fremdkörper-Riesenzellen.
Diagnostik
Synonyms -
Granulome,granulomatös,granulomatöse
|